Pocetna Stranica › Forums › FORUM › Soli
-
AuthorPosts
-
January 23, 2025 at 9:02 am #1505
Imam jedno pitanje, ovaj zadatak me malo zbunjuje
Ako se kiselina i baza pomešaju u istom molarnom odnosu koji od navedenih rastvora reaguje kiselo?
a) HCl+NaOH
b) H2CO3+KOH
c)HF+NaOH
d) H3PO4+Ca(OH)2
e) H2SO4+ Al(OH)3
Ne znam da li se pitanje odnosi na neutralizaciju ili hidrolizu, jer ako je za neutralizaciju po meni tačni su odgovori pod b) i d) jer se grade kisele soli KHCO3 i CaHPO4 i te reakcije su u istom molarnom odnosu. A ako se radi o hidrolizi onda bi po meni odgovor bio pod e) jer je so nastala od jake kiseline i slabe baze nema veze što se gradi AlOHSO4 da bi bila rekacija u istom molarnom odnosu, ali po meni ako su mislili na hidrolizu trebali su da napišu koja so u VODENOM rastvoru reaguje kiselo. Zato sam jako zbunjena i želim da čujem Vaša mišljenja i hvala Vam unapred!!!
January 24, 2025 at 9:41 am #1509Mislim da u skoli se ima tendencija klasifikovanja hemijskih reakcija…reakcija neutralizacije…reakcija hidrolize…ali u realnom hemijskom svetu stvari nikad nisu bas potpuno klasifikovane…
Neutralizacija…sigurno je da se dogadja neutralizacija ali nepotpuna…i ono sto dobijemo ima tendenciju da hidrolizira.
Kiseli rastvor (ako pod time podrazumevamo da ce pH rastvora biti manji od 7) je jedino onaj pod e)
E sad, b) i d)
H2CO3 je slaba kiselina…i ako napravimo so KHCO3…a toliko mozemo jer toliko baze imamo…rastvor tesko moze da bude kiseo jer pre ce HCO3- da “dograbi” H+ iz vode nego sto ce da otpusti H+. (Recimo iz literature se vidi da je 0.1 M rastvor KHCO3 bazan pH=8.2)
d)
U istoj smo dilemi kada napravimo CaHPO4…mislim da ce rastvor biti blago bazan jer u vodi pre ce se napraviti (H2PO4)- nego (PO4)3-
January 24, 2025 at 1:06 pm #1514Da dodam jos nesto…
Ponekad je korisno posmatrati titracione krive..npr titracija H2CO3 sa jakom bazom…zavrsna tacka titracije nam govori kakav ce biti pH…
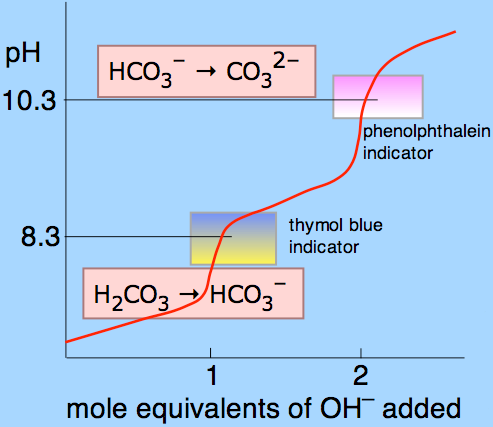
vidimo da na pH=8.3 je ona tacka kada smo “pretvorili” sav H2CO3 u HCO3-
January 24, 2025 at 1:15 pm #1515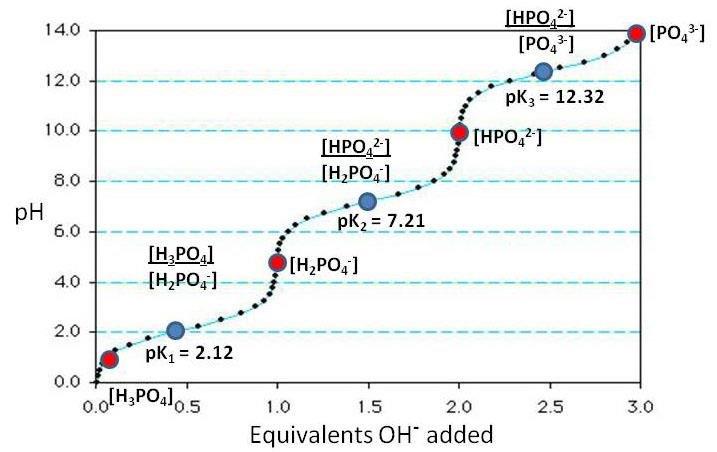
na pH=10 smo dosli do CaHPO4…
-
AuthorPosts
You must be logged in to reply to this topic.
